Оглавление
Общие сведения
Фенилкетонурия (болезнь Феллинга, фенилпировиноградная олигофрения) – врожденная, генетически обусловленная патология, характеризующаяся нарушением гидроксилирования фенилаланина, накоплением аминокислоты и ее метаболитов в физиологических жидкостях и тканях с последующим тяжелым поражением ЦНС. Фенилкетонурия впервые описана А.
Феллингом в 1934 г.; встречается с частотой 1 случай на 10 000 новорожденных. В неонатальном периоде фенилкетонурия не имеет клинических проявлений, однако поступление фенилаланина с пищей вызывает манифестацию заболевания уже в первом полугодии жизни, а в дальнейшем приводит к тяжелым нарушениям развития ребенка. Именно поэтому пресимптоматическое выявление фенилкетонурии у новорожденных является важнейшей задачей неонатологии, педиатрии и генетики.
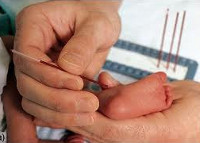
Фенилкетонурия
Причины фенилкетонурии
В основе заболевания лежит генетический дефект – мутация гена 12-й хромосомы (98% всех случаев фенилкетонурии). Это так называемая классическая фенилкетонурия.
Ген кодирует количество фермента фенилаланин-4-гидроксилазы. Фермент отвечает за превращение аминокислоты фенилаланина в организме человека в тирозин в клетках печени.
Фенилаланин – это аминокислота, которая содержится в белковых продуктах (мясо, рыба, молоко, яйца и другие).
При мутации гена количество фермента снижается, что приводит к накоплению фенилаланина и продуктов промежуточного метаболизма в тканях организма. Организм пытается избавиться от фенилаланина и продуктов его распада, выводя их с мочой.
Подобные нарушения обмена веществ приводят к нарушению строения нервных проводников, снижению образования нейромедиаторов. Все это, наряду с прямым токсическим действием избытка фенилаланина, приводит к развитию умственных нарушений, являющихся основным проявлением заболевания.
Фенилкетонурия наследуется по аутосомно-рецессивному типу, то есть не зависит от пола, и возникает при совпадении двух патологических генов от отца и матери.
Они имеют те же клинические проявления, но не поддаются лечению диетой. Такие варианты относят к атипичному течению заболевания. Среди них принято выделять фенилкетонурию II и III.
Генетический дефект при фенилкетонурии II располагается в 4-й хромосоме, при III – в 11-й хромосоме.
Симптомы
У детей с фенилкетонурией светлые волосы, бледная кожа и голубые глаза.
Ребенок с фенилкетонурией рождается внешне здоровым, то есть ничем не отличается от других детей. С поступлением пищи в организм начинается попадание белка, а значит и фенилаланина. Последний постепенно накапливается, и обычно к 2 месяцам жизни появляются первые симптомы: вялость или беспокойство, отсутствие интереса к окружающему миру, срыгивания, изменения мышечного тонуса.
К 4-6 месяцам становится очевидной задержка психического развития. Ребенок не следит за игрушкой, не реагирует на звук, не узнает родителей.
Чем дольше продолжается поступление фенилаланина в организм с едой, тем выраженнее нарушения в психической и мыслительной сферах. Развитие речи резко задерживается. Иногда словарный запас может ограничиваться несколькими словами.

Если диагноз не будет выставлен и не будет начато лечение, то к 3-4 годам умственные нарушения достигнут степени идиотии (самая тяжелая степень олигофрении).
Особенностью клинического течения фенилкетонурии является необратимость возникших психических и интеллектуальных изменений. То есть при позднем выявлении помочь таким деткам уже нельзя – на всю жизнь они остаются умственно отсталыми.
Физическое развитие также отстает: дети позже начинают держать голову, переворачиваться, сидеть. Когда такие дети начинают ходить, то при этом они широко расставляют ножки, сгибая их одновременно в коленных и тазобедренных суставах.
Походка покачивающаяся, мелкими шажками. В положении сидя дети принимают «позу портного» — сгибают и руки, и ноги, поджимая последние под себя. Обычно объем головы меньше, чем в норме. Может быть выраженная микроцефалия: маленькая голова.
Из других неврологических симптомов возможны нарушения мышечного тонуса, судорожные припадки. Эпилептические приступы обычно появляются в возрасте 1,5 лет и приводят к еще большему прогрессированию нарушений интеллекта.
У части больных фенилкетонурией появляются непроизвольные движения в конечностях, дрожание (гиперкинезы). В движениях нет плавности и согласованности, нарушается равновесие.
Кроме ряда психических и интеллектуальных изменений, фенилкетонурию характеризуют следующие симптомы:
- специфический «мышиный» запах (или запах плесени) от ребенка: этот симптом характерен только для фенилкетонурии. Запах появляется в результате выделения продуктов метаболизма фенилаланина (фенилпировиноградной, фенилмолочной, фенилуксусной кислот) через кожу и с мочой;
- кожные проявления: дерматиты, экзема, просто шелушение (возникают по той же причине, что и «мышиный» запах);
- позднее прорезывание зубов: у таких детей первые зубы могут появиться после 18 месяцев, эмаль недоразвита;
- нарушение пигментации: у таких детей обычно голубые глаза, очень светлая кожа и волосы в результате снижения количества меланина (его содержание зависит от метаболизма фенилаланина). Из-за этого у таких детей наблюдается повышенная чувствительность к солнечному свету;
- вегетативные симптомы: пониженное артериальное давление, повышенная потливость, запоры, акроцианоз (синюшность кистей и стоп);
- нередко фенилкетонурия сопровождается врожденными пороками сердца.
Атипичные случаи фенилкетонурии, связанные с нарушением деятельности других ферментов, участвующих в метаболизме фенилаланина, кроме умственных изменений характеризуются развитием мышечной слабости во всех конечностях с одновременным повышением мышечного тонуса, спастическим тетрапарезом. Также при этих формах развивается слюнотечение, приступы повышения температуры.
У взрослых людей, страдающих фенилкетонурией, возможно появление судорожных припадков, нарушений координации, дрожания в конечностях, ухудшения памяти и внимания, возникновение депрессии. Обычно подобные симптомы возникают при несоблюдении элиминационной диеты.
Диагностика

Скрининговые тесты на содержание фенилаланина всем новорожденным проводят в роддоме.
В связи с тем, что фенилкетонурия сопровождается развитием необратимых умственных нарушений, во многих странах мира, в том числе и в России, принято использовать скриниг-методы диагностики. Что это означает? Всем без исключения новорожденным детям в роддоме проводят экспресс-тесты на содержание фенилаланина.
Для этого берут капиллярную кровь (из пятки) на 4-5-й день жизни ребенка (у недоношенных на 7-й), наносят на специальный бумажный бланк и отправляют в лабораторию, где по определенным изменениям врач-лаборант делает выводы о содержании фенилаланина в крови. Отрицательный тест говорит об отсутствии фенилкетонурии.
Если тест оказывается положительным, то тогда проводят дополнительные исследования для определения содержания фенилаланина в крови и моче (хроматографию, флюориметрию). Концентрацию фенилаланина в крови и моче регулярно проверяют при проведении лечения, чтобы контролировать эффективность диеты и корригировать ее при необходимости.
Возможно проведение генетического исследования для подтверждения мутации в гене, отвечающем за фенилаланин-4-гидроксилазу.
Подобное исследование возможно в качестве пренатальной диагностики, то есть на этапе беременности (берут околоплодные воды путем пункции).
Это инвазивное исследование делают по строгим показаниям (например, наличие больного фенилкетонурией ребенка в семье). Выявление генетического дефекта у плода позволяет прервать беременность.
На сегодняшний день самым эффективным и распространенным способом лечения фенилкетонурии является элиминационная диета: диета с исключением продуктов, содержащих фенилаланин. Если ее строго придерживаться в первые годы жизни ребенка, когда развитие нервной системы еще продолжается, то можно вырастить здорового и полноценного человека.
Очень важно исключение фенилаланина именно в первый год жизни, когда наиболее активно развивается нервная система. Если элиминационная диета назначается после года, умственные нарушения не излечиваются. Каждый месяц первого года жизни без применения диеты обходится ребенку безвозвратной потерей около 4 баллов IQ.
Обычно достаточно придерживаться диеты до 16-18 лет, после этого возраста организм становится менее чувствительным к токсическому действию фенилаланина, и возможно расширение рациона питания. Включение новых продуктов необходимо проводить под контролем содержания фенилаланина в крови. Иногда требуется пожизненное строгое соблюдение диеты.
Степень строгости диеты зависит от концентрации фенилаланина в крови у ребенка. При его уровне до 2-6 мг% (120-360 мкмоль/л) диета не назначается, выше этого показателя – обязательна.
Суть диеты заключается в исключении белковых продуктов.
Отказ от грудного вскармливания не обязателен, но в этом случае кормящая мать должна строго придерживаться элиминационной диеты, потому что грудное молоко содержит белок (соответственно и фенилаланин). Вопрос о возможности грудного вскармливания решается индивидуально!!!
В России обеспечение лечебным питанием детей, больных фенилкетонурией, по закону бесплатное.
Больным фенилкетонурией противопоказаны следующие продукты: мясо, рыба (и морепродукты), орехи, творог, твердый сыр, бобовые, яйца, изделия из пшеничной муки, гречневая и манная крупа, овсяные хлопья.
Фенилкетонурия является заболеванием с аутосомно-рецессивным характером наследования. Это означает, что для развития клинических признаков фенилкетонурии ребенок должен унаследовать по одной дефектной копии гена от обоих родителей, являющихся гетерозиготными носителями мутантного гена.
Чаще всего к развитию фенилкетонурии приводит мутация гена, кодирующего фермент фенилаланин-4-гидроксилазу и расположенного на длинном плече 12 хромосомы (локус12q22-q24.1). Это, так называемая, классическая фенилкетонурия I типа, составляющая 98% всех случаев заболевания. Гиперфенилаланинемия может достигать 30 мг% и выше. При отсутствии лечения данный вариант фенилкетонурии сопровождается глубокой умственной отсталостью.
Кроме классической формы, различают атипичные варианты фенилкетонурии, протекающие с той же клинической симптоматикой, но не поддающиеся коррекции диетотерапией. К ним относятся фенилкетонурия II типа (недостаточность дегидроптеринредуктазы), фенилкетонурия III типа (дефицит тетрагидробиоптерина) и другие, более редкие варианты.
Вероятность рождения ребенка, больного фенилкетонурией, повышается при заключении близкородственных браков.
Основные принципы диеты при фенилкетонурии
Уважаемые родители!
Фенилаланин (ФА) — это эгзогенная незаменимая аминокислота, необходимая для нормального роста и развития, которая поступает в организм с пищей. У пациентов с ФКУ доза фенилаланина ограничивается до количества, которое зависит от индивидуальной толерантности к ФА.
Низкобелковая диета позволяет удерживать концентрацию ФА в сыворотке крови больного уровне на безопасном для ЦНС уровне. Этот уровень определен для каждой возрастной группы. Для грудного возраста ФА должен быть на уровне 2-4мг%, проверка уровня концентрации ФА в сыворотке крови пациента проводится 1 раз/в неделю до 6 месяца жизни.
Чтобы содержание фенилаланина находилось на определённом „безопасном” уровне, диета должна состоять из лечебных препаратов с низким содержанием фенилаланина или без него (которые удовлетворяют потребность в белке на 70-80%), и такого количества натуральных продуктов, чтобы удовлетворить потребности организма в белке, минеральных компонентах, витаминах и фенилаланине, учитывая основные возрастные потребности ребёнка.
- Уменьшение дозы фенилаланина согласно индивидуальной толерантности фенилаланина, что означает уменьшение дозы натурального белка в суточном рационе
- Обеспечение соответствующей для нормального развития дозы белка (дополнительный белок без фенилаланина) из продуктов лечебного питания ФКУ
- Обеспечение соответствующей дозы энергии с использованием специальных низкобелковых продуктов
- Обеспечение соответствующей дозы витамин, макро- и микроэлементов – главным образом из препаратов ФКУ и других источников.
|
|
|
У пациентов с ФКУ количество потребляемого белка из натуральных продуктов не может превысить установленной нормы. В связи с этим у маленьких детей и у старших преобладающая часть потребности в белке, т.е. около 80%, должно быть погашено смесями, не содержащими фенилаланин, обогащёнными минеральными ингредиентами.
Диета грудного ребёнка с ФКУ базируется на смесях (препаратах) без фенилаланина, которые являются главными источниками белка, витаминов, микро- и макроэлементов. Грудное молоко и молочная смесь для младенцев дополняют эту диету необходимым для роста фенилаланином. Количество препарата ФКУ, грудного молока или молочных смесей надо систематически изменять в зависимости от индивидуальной толерантности фенилаланина, а также и от потребностей растущего организма.
только смесь аминокислот («белковый эквивалент») в сочетании с витаминами и минералами. Необходимое количество белка свободного от фенилаланина поступает в организм из низкоэнергетических напитков: фруктовые соки, фруктово-овощные соки. Такая смена режима и рациона питания может повлиять на обмен аминокислот.
В связи с тем, что смеси свободные от фенилаланина содержат мало калорий, а питание должно быть сбалансированным, т.е. отвечать определённым соотношениям содержания жиров и углеводов (основных источников энергии) таким образом, чтобы полностью удовлетворить суточную потребность организма в энергии, целесообразным становится обогащение суточного рациона иными высокоэнергетическими пищевыми прдуктами. Это стало возможным благодаря наличию на рынке большого количества специализированных низкобелковых и частично свободных от фенилаланина продуктов.
Дневная доза смеси ФКУ зависит от возраста ребёнка, массы тела, общего состояния здоровья и индивидуальной суточной толерантности фенилаланина. Очень важно, чтобы рекомендуемое суточное количество смеси не давать в один приём, напр.
утром. Такой способ подачи смеси может привести к колебаниям аминокислотного равновесия или к симптомам нетолерантности препарата. Суточную дозу смеси необходимо поделить на 3-4 приёма в течении дня. Препарат следует принимать во время еды.
Суточное потребление фенилаланина из пищевых продуктов должно быть ограничено до такого количества, чтобы контролируемый уровень концентрации фенилаланина в сыворотке крови не превышал „безопасного для ЦНС” уровня, т.е.
2-4мг/дл, это и есть индивидуальная суточная толерантность фенилаланина.
С целью полного удовлетворения потребностей ребёнка с фенилкетонурией, и поддержания на допустимом уровне употребляемого из продуктов натурального белка и фенилаланина следует все пищевые продукты отмерять и взвешивать, а также выбирать продукты с самым низким содержанием фенилаланина.
Учитывая факт, что диета пациентов с ФКУ должна предусматривать ограничение дозы фенилаланина до количества безопасного для ЦНС, очень важно одновременно обеспечить поставку основных ингредиентов питания: белка, углеводов, жиров, а также витаминов, микро- и макроэлементов, энергии и объема жидкости согласно рекомендациям для определенных возрастных групп.
Очень часто повышение концентрации фенилаланина в сыворотке крови ребёнка означает, что количество употребляемого ребёнком фенилаланина значительно превышает рекомендуемую суточную дозу. Причиной может быть также проблема с употреблением препарата ФКУ.
Хронический недостаток энергии, также как и недобор белка ускоряют процесс разрушения собственных белков организма (катаболические процессы).
Разрушение белков и увеличение концентрации фенилаланина могут быть вызваны инфекционным процессом, который протекает с повышением температуры тела, рвотой, поносом, снижением аппетита, хирургическими операциями (интенсификация катаболических процессов, увеличение потребности в энергии).

В таких случаях следует увеличить поступающее в организм количество энергии. Во время болезни ребёнка следует обратить внимание на количество употребляемых калорий, так как дефицит энергии является основной причиной ускорения катаболизма белков, а вследствие этого повышается уровень фенилаланина.
При инфекциях следует увеличить поступление энергии на 20 – 30%. При высокой температуре необходимо увеличить количество энергии на 12% на каждый 1 градус температуры. При поносе или рвоте следует на 1-2 дня отказаться от диеты ФКУ, а после выздоровления постепенно к ней вернуться.
При быстром приросте массы тела ребёнка может появиться необходимость в дополнительной порции питания или препарата. Невнимательный подход к этим потребностям и несоблюдение основных требований диеты может отрицательным образом повлиять на уровень фенилаланина в крови пациента.
Родители должны постоянно восполнять свои знания о ФКУ и использовать их в практике ежедневной диеты. Обучая ребёнка правилам правильного питания, родители должны подчёркивать значимость систематического приёма пищи и употребления исключительно разрешенных продуктов. Ребенку нужно систематически объяснять в доступной форме необходимость отказа от высокобелковых продуктов. Важно также, чтобы ребёнок мог отказаться от угощения ровесников и умел определять сходства и отличия в выборе продуктов.
Диетическое питание для детей с фенилкетонурией является единственным эффективным методом лечения. Из рациона больного необходимо исключить продукты с высоким содержанием белка. Но жизнь без белка невозможна, ведь он является пластическим материалом, из которого строятся все органы. Поэтому, когда ученые-биохимики получили гидролизат белка, полностью лишенный фенилаланина — берлофен, в истории фенилкетонурии открылась новая страница. И тысячи детей получили возможность вырасти здоровыми, не отставая от своих сверстников с нормальным аминокислотным обменом.
В настоящее время выпускаются специализированные лечебные продукты для питания детей, больных фенилкетонурией, которые обеспечивают потребности в белковом компоненте. Это «Афенилак», «Лофеналак», «Аналог ХР» для детей первого года жизни, приближенные по составу к грудному молоку. Также для детей с фенилкетонурией показаны смеси «Тетрафен», «Триафен», «Фенил-фри», «Нофелан», «Фенил-40», «Лактанал», малобелковые или безбелковые овощные и фруктовые консервы, обогащенные витаминами и минеральными солями, для употребления в виде прикорма.
Патогенез фенилкетонурии
В основе классической формы фенилкетонурии лежит недостаточность фермента фенилаланин-4-гидроксилазы, участвующего в конверсии фенилаланина в тирозин в митохондриях гепатоцитов. В свою очередь, производный тирозина – тирамин является исходным продуктом для синтеза катехоламинов (адреналина и норадреналина), а дийодтирозин – для образования тироксина. Кроме этого, результатом метаболизма фенилаланина служит образование пигмента меланина.
Наследственная недостаточность фермента фенилалаиин-4-гидроксилазы при фенилкетонурии приводит к нарушению окисления фенилаланина, поступающего с пищей, в результате чего его концентрация в крови (фенилаланинемия) и спинномозговой жидкости значительно возрастает, а уровень тирозина соответственно падает. Избыточное содержание фенилаланина устраняется путем повышенной экскреции с мочой его метаболитов – фенилпировиноградной, фенилмолочной и фенилуксусной кислот.
Нарушение обмена аминокислот сопровождается нарушением миелинизации нервных волокон, снижением образования нейромедиаторов (дофамина, серотонина и др.), запускающими патогенетические механизмы задержки умственного развития и прогредиентное слабоумие.
Диагностика фенилкетонурии
В настоящее время диагностика фенилкетонурии (а также галактоземии, врожденного гипотиреоза, адрено-генитального синдрома и муковисцидоза) входит в программу неонатального скрининга, осуществляемого всем новорожденным.
Скрининг-тест проводится на 3-5 день жизни доношенного и 7 день жизни недоношенного ребенка путем забора образца капиллярной крови на специальный бумажный бланк. При обнаружении гиперфенилаланемии более 2,2 мг% ребенка направляют к детскому генетику для повторного обследования.
Для подтверждения диагноза фенилкетонурии проверяется концентрация фенилаланина и тирозина в крови, определяют активность печеночных ферментов (фенилаланингидроксилазы), выполняется биохимическое исследование мочи (определение кетоновых кислот), метаболитов катехоламинов в моче и др. Дополнительно проводится ЭЭГ и МРТ головного мозга, осмотр ребенка детским неврологом.
Генетический дефект при фенилкетонурии может быть обнаружен еще на этапе беременности в ходе инвазивной пренатальной диагностики плода (хорионбиопсии, амниоцентеза, кордоцентеза).
Дифференциальный диагноз фенилкетонурии проводят с внутричерепной родовой травмой новорожденных, внутриутробными инфекциями, другими нарушениями обмена аминокислот.
Симптомы фенилкетонурии
Новорожденные с фенилкетонурией не имеют клинических признаков заболевания. Обычно манифестация фенилкетонурии у детей происходит в возрасте 2-6 месяцев. С началом кормления в организм ребенка начинает поступать белок грудного молока либо его заменителей, что приводит к развитию первых, неспецифических симптомов – вялости, иногда – беспокойства и гипервозбудимости, срыгивания, мышечной дистонии, судорожного синдрома. Одним из ранних патогномоничных признаков фенилкетонурии служит упорная рвота, которая нередко ошибочно расценивается как проявление пилоростеноза.
Ко второму полугодию становится заметным отставание ребенка в психомоторном развитии. Ребенок становится менее активным, безучастным, перестает узнавать близких, не пытается садиться и вставать на ножки. Аномальный состав мочи и пота обусловливают характерный «мышиный» запах (запах плесени), исходящий от тела. Часто наблюдается шелушение кожи, дерматиты, экзема, склеродермия.
У детей с фенилкетонурией, не получающих лечения, выявляется микроцефалия, прогнатия, позднее (после 1,5 лет) прорезывание зубов, гипоплазия эмали. Отмечается задержка речевого развития, а к 3-4 годам выявляется глубокая олигофрения (идиотия) и практически полное отсутствие речи.
Дети с фенилкетонурией имеют диспластическое телосложение, нередко – врожденные пороки сердца, вегетативные дисфункции (потливость, акроцианоз, артериальную гипотонию), страдают запорами. К фенотипическим особенностям детей, страдающих фенилкетонурией, следует отнести светлую кожу, глаза и волосы. Для ребенка с фенилкетонурией характерны специфическая поза «портного» (согнутые в суставах верхние и нижние конечности), тремор рук, шаткая, семенящая походка, гиперкинезы.
Клинические проявления фенилкетонурии II типа характеризуются тяжелой степенью умственной отсталости, повышенной возбудимостью, судорогами, спастическим тетрапарезом, сухожильной гиперрефлексией. Прогрессирование заболевание может приводить к гибели ребенка в возрасте 2-З лет.
При фенилкетонури III типа развивается триада признаков: микроцефалия, олигофрения, спастический тетрапарез.
Лечение фенилкетонурии
Основополагающим фактором в лечении фенилкетонурии является соблюдение диеты, ограничивающей поступление белка в организм. Лечение рекомендуется начинать при концентрации фенилаланина {amp}gt;6 мг%. Для грудных детей разработаны специальные смеси – Афенилак, Лофенилак; для детей старше 1 года – Тетрафен, Фенил-фри; старше 8 лет – Максамум-ХР и др. Основу диеты составляют низкобелковые продукты – фрукты, овощи, соки, белковые гидролизаты и аминокислотные смеси. Расширение диеты возможно после 18 лет в связи с возрастанием толерантности к фенилаланину. В соответствии с российским законодательством обеспечение лиц, страдающих фенилкетонурией, лечебным питанием, должна осуществляться бесплатно.
Больным назначается прием минеральных соединений, витаминов группы В и др.; по показаниям – ноотропные средства, антиконвульсанты. В комплексной терапии фенилкетонурии широко используется общий массаж, ЛФК, иглорефлексотерапия.
Дети, страдающие фенилкетонурией, находятся под наблюдением участкового педиатра и психоневролога; нередко нуждаются в помощи логопеда и дефектолога. Необходим тщательный мониторинг нервно-психического статуса детей, контроль уровня фенилаланина в крови и показателей электроэнцефалограммы.
Атипичные формы фенилкетонурии, не поддающиеся лечению диетой, требуют назначения гепатопротекторов, противосудорожных средств, заместительной терапии леводопой, 5-гидрокситриптофаном.
Прогноз и профилактика фенилкетонурии
Проведения массового скрининга на фенилкетонурию в неонатальном периоде позволяет организовать раннюю диетотерапию и предотвратить тяжелые церебральные повреждения, нарушения функции печени. При раннем назначении элиминационной диеты при классической фенилкетонурии прогноз развития детей хороший. При поздно начатом лечении прогноз в отношении умственного развития неблагоприятный.
Профилактика осложнений фенилкетонурии заключается в проведении массового скрининга новорожденных, раннего назначения и длительного соблюдения диетического питания.
С целью оценки риска рождения ребенка с фенилкетонурией предварительное генетическое консультирование должны пройти супружеские пары, уже имеющие больного ребенка, состоящие в кровнородственном браке, имеющие родственников с данным заболеванием. Женщины с фенилкетонурией, планирующие беременность, должны соблюдать строгую диету до зачатия и во время беременности для исключения повышения уровня фенилаланина и его метаболитов и нарушения развития генетически здорового плода. Риск рождения ребенка с фенилкетонурией у родителей-носителей дефектного гена, составляет 1:4.
